GIUNTA REGIONALE
Omissis
LA GIUNTA REGIONALE
Vista la legge 27 dicembre 2006 n. 296 articolo 1 comma 796 e successivi;
Richiamati
- la D.G.R. nr. 224 del 13.03.2007 recante la “Approvazione dell’accordo tra il Ministero della Salute, il Ministero dell’Economia e delle Finanze e la Regione Abruzzo per l’approvazione del piano di rientro di individuazione degli interventi per il perseguimento dell’equilibrio economico ai sensi dell’art. 1 comma 180, della legge 30.12.2004 n. 311;
- il Piano di risanamento del Sistema Sanitario Regionale 2007-2009, quale parte integrante del predetto accordo;
Considerato che il predetto Piano di Risanamento - al punto 2.1.3.1.5 dell’Obiettivo L1 - prevede:
1. l’istituzione della Commissione Terapeutica Regionale;
2. che la predetta Commissione Terapeutica abbia - tra l’altro - il compito di definire il Prontuario Terapeutico Regionale;
3. che la scelta dei farmaci da introdurre nel Prontuario debba essere effettuata sulla base dei seguenti criteri:
- efficacia clinica dimostrata da studi controllati;
- Sicurezza (favorevole rapporto rischio/beneficio);
- economicità (rapporto costo/beneficio favorevole in relazione a farmaci di pari efficacia clinica);
- valutazione dell’innovatività in termini di reale vantaggio terapeutico;
Richiamate:
- la DGR n. 663 del 09.07.2007 di istituzione ed attivazione della Commissione Regionale del Farmaco;
- la DG8/111 del 24.10.2007 di recepimento della approvazione da parte della Commissione Regionale del Farmaco dei criteri di elaborazione del PTR nella Regione Abruzzo nonché della prima stesura del Prontuario Terapeutico medesimo;
Richiamati altresì i predetti criteri di elaborazione del PTR (all. A) - parte integrante e sostanziale del presente atto - ove è espressamente previsto che:
- il Prontuario Regionale al di là del mero aspetto economicistico legato all’acquisizione del farmaco ed alle gare d’appalto - abbia esclusivamente una funzione di riferimento e di guida per le decisioni che possono/devono essere assunte nelle singole realtà locali (sia a livello di singola struttura che di ASL) in relazione al livello assistenziale, alla sua organizzazione ed alla sua complessità;
- nell’ottica di una corretta promozione all’utilizzo ed alla prescrizione dei farmaci generici sia nelle realtà ospedaliere che nella continuità ospedale/territorio, l’ambito di discrezionalità e variabilità delle scelte delle singole Commissioni Terapeutiche aziendali - laddove esistenti - sia ovviamente limitato dal rispetto di alcuni criteri di base, tra cui assume particolare rilevanza il seguente assunto: “...i farmaci generici sono prioritari (ed eventualmente esclusivi) per tutte le classi terapeutiche dove esistono...”;
- nell’ambito dei Prontuari locali, la scelta di farmaci che per condizioni cliniche prevedono una continuità prescrittiva sul territorio richieda peculiare ponderazione, in quanto gli stessi necessitano di contribuire a garantire alla prescrizione della medicina generale le stesse caratteristiche di razionalità complessiva (clinica, terapeutica, organizzativa, economica) richieste a livello ospedaliero;
Considerato opportuno ribadire e fare proprio quanto già assunto nella prefata DG8/111 del 24.10.2007, ossia che:
1. relativamente ad alcuni farmaci per cui siano richieste particolari precauzioni d’uso legate al profilo di sicurezza ed alla maneggevolezza del farmaco stesso, ovvero siano destinati ad una particolare fascia di pazienti, o ancora abbiano un costo molto elevato, il Prontuario possa essere implementato con specifiche note limitative o schede di richiesta motivata o schede di monitoraggio, al fine di verificare puntualmente che il farmaco sia prescritto ed utilizzato nelle condizioni autorizzate;
2. una corretta implementazione della politica di regionale di impiego dei prontuari, necessita dell’attivazione - nelle diverse ASL della Regione - di Commissioni Farmaceutiche ad hoc, le quali consentano di espletare quelle attività di formazione culturale che costituiscono la principale finalità del Prontuario Terapeutico Regionale, mediante la Direzione Sanitaria e la Farmacia interna Ospedaliera, che costituiscono a tal fine i principali organi di riferimento della Commissione medesima;
Dato atto che:
- nel corso della riunione tenutasi il 15.02.2008 la Commissione Regionale del Farmaco ha proceduto ad effettuare un aggiornamento del PTR di cui alla citata DG8/111 del 24.10.2007 e che detto aggiornamento è stato recepito con Determina del Servizio Assistenza Farmaceutica DG8/42 del 04.04.2008;
- nel corso della riunione tenutasi il 14.05.2008 la Commissione Regionale del Farmaco ha proceduto ad effettuare un aggiornamento del PTR di cui alla citata DG8/42 del 04.04.2008 e che detto aggiornamento è stato recepito con Determina del Servizio Assistenza Farmaceutica DG8/71 del 29.05.2008;
Dato atto che il PTR siccome aggiornato alla data del 14.05.2008, risulta composto da:
- Introduzione e criteri di riferimento;
- Abbreviazioni, acronimi e legenda PTR;
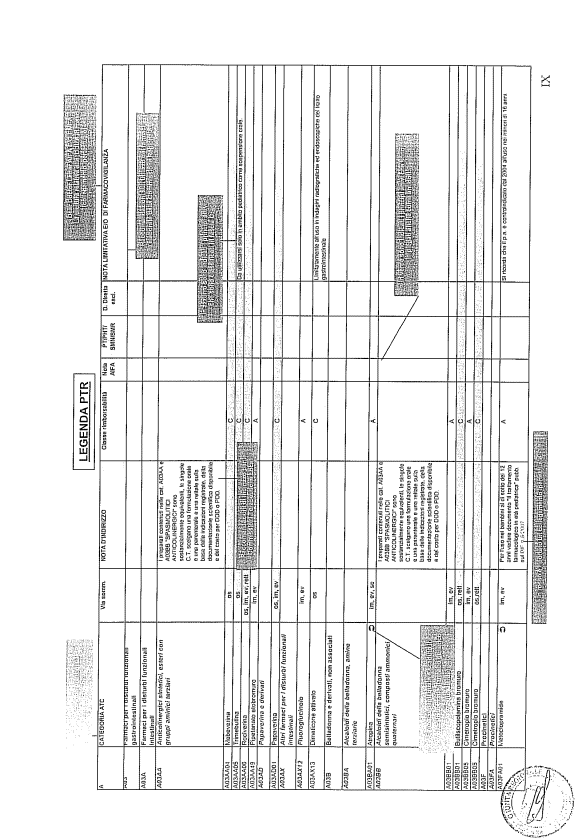
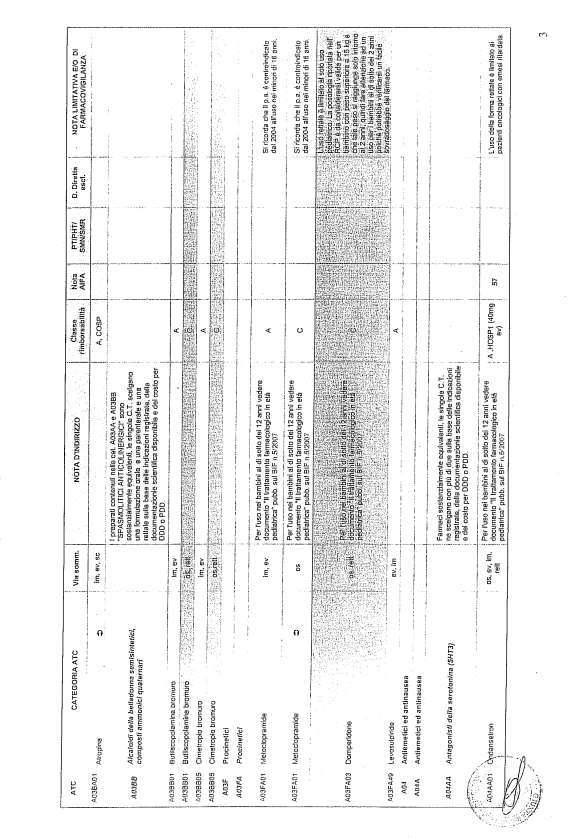
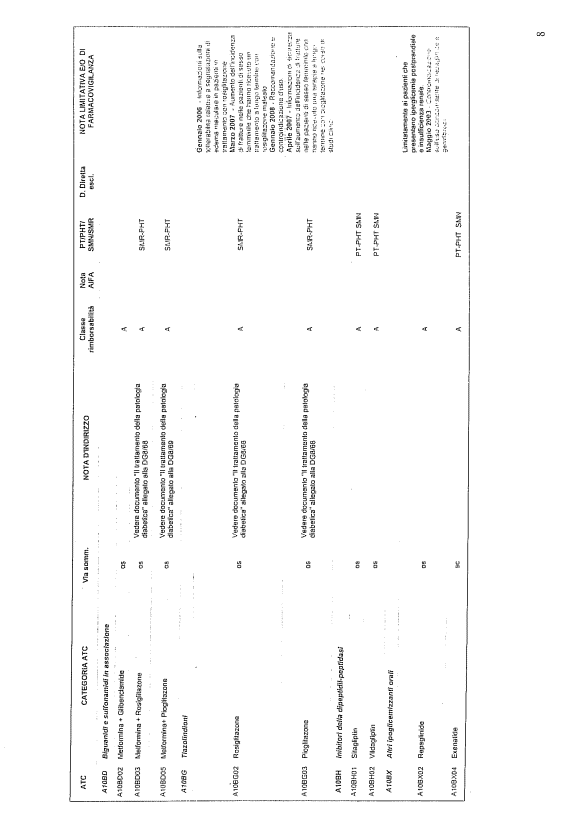
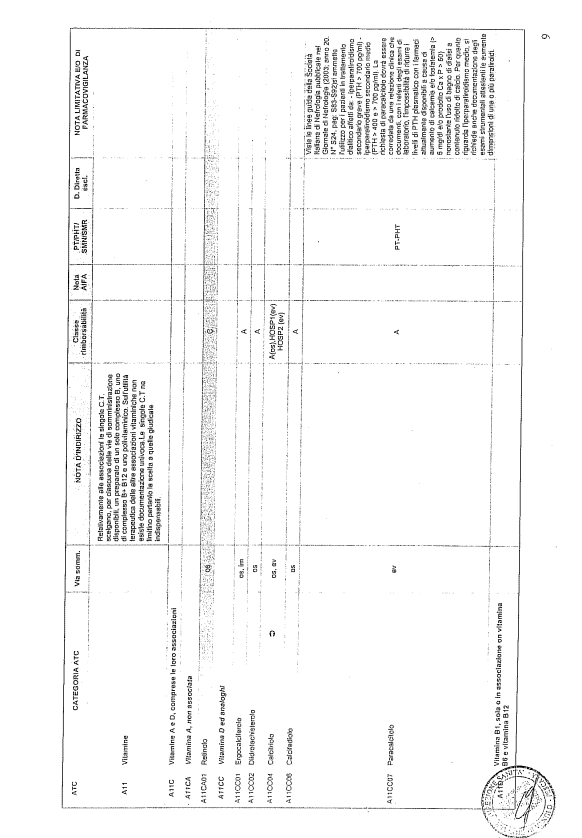
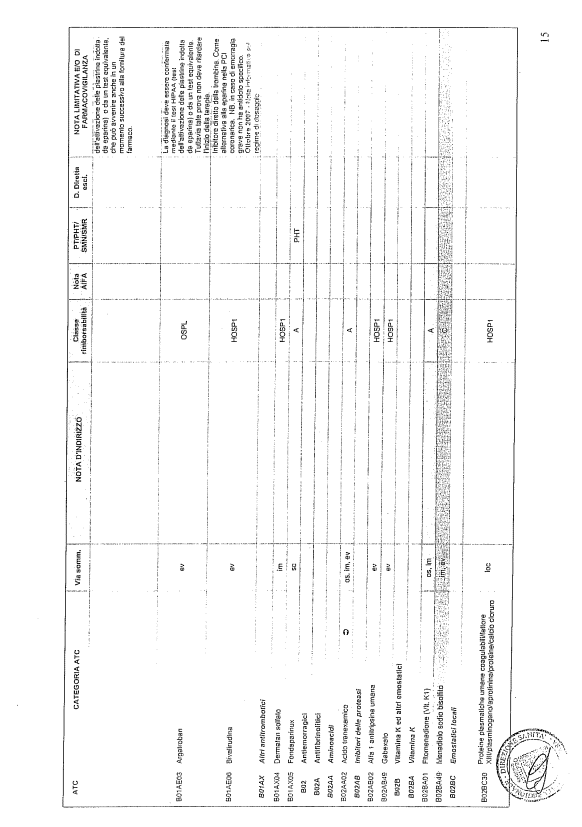
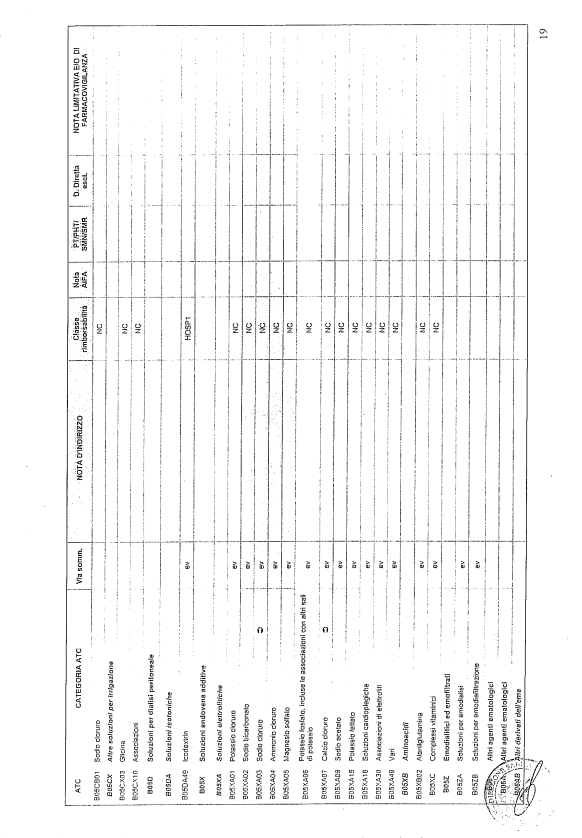
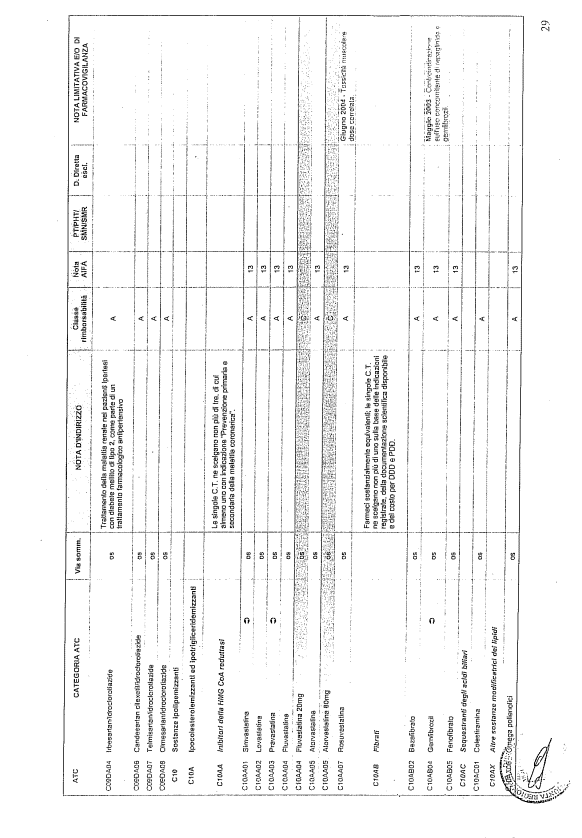
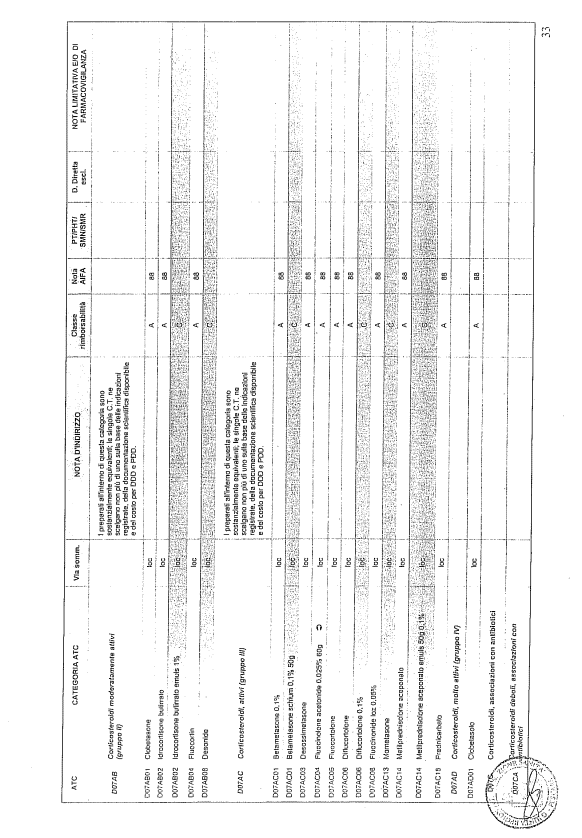
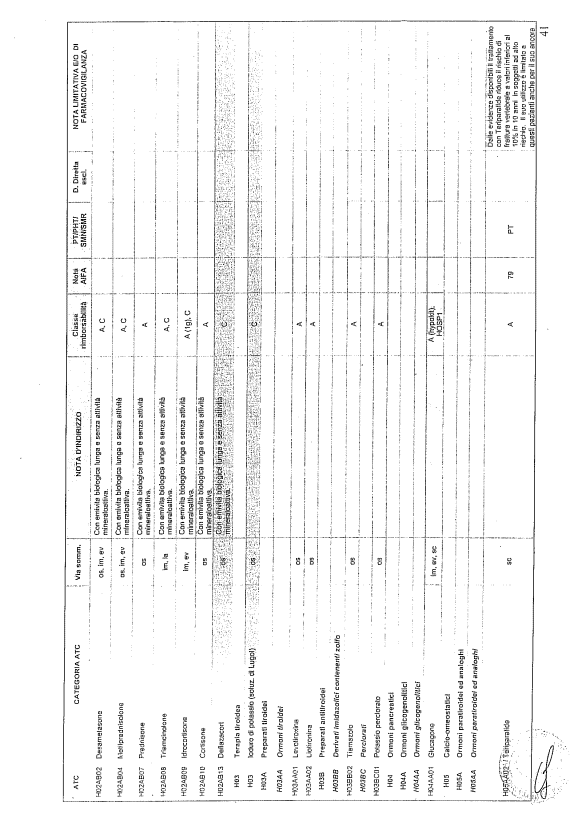
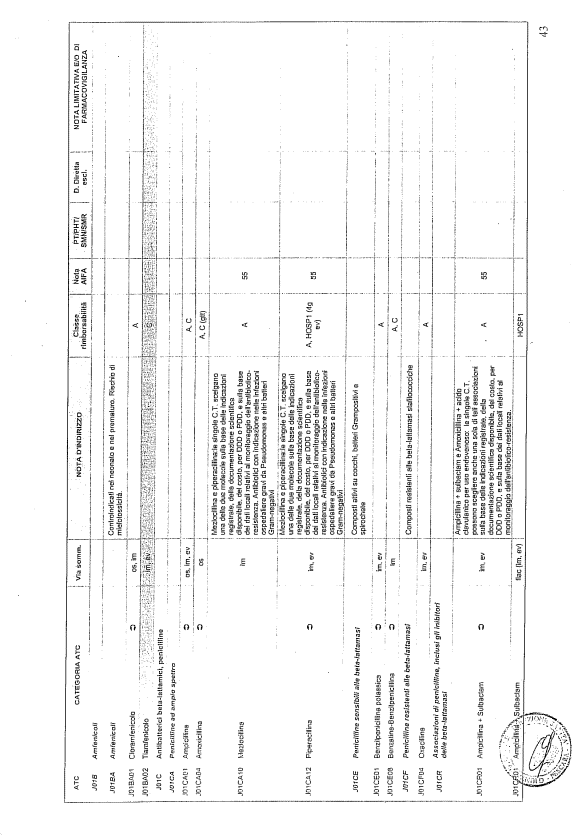
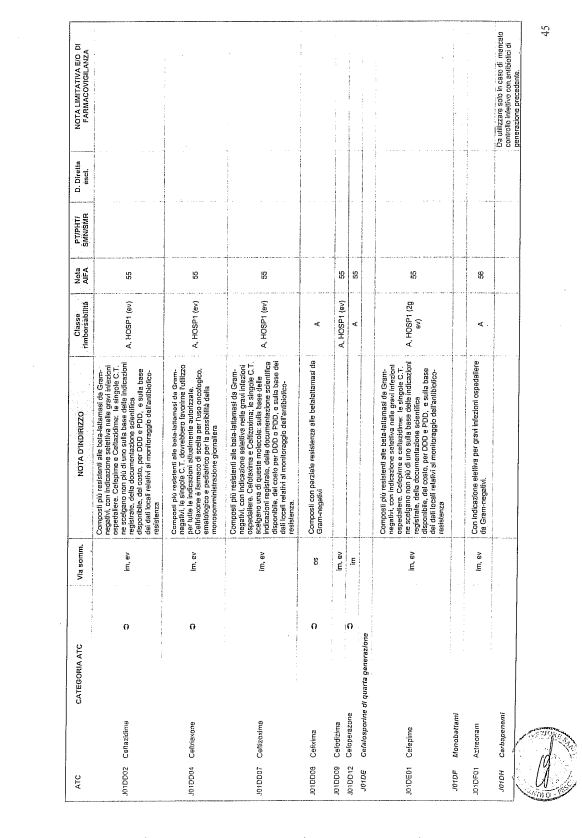
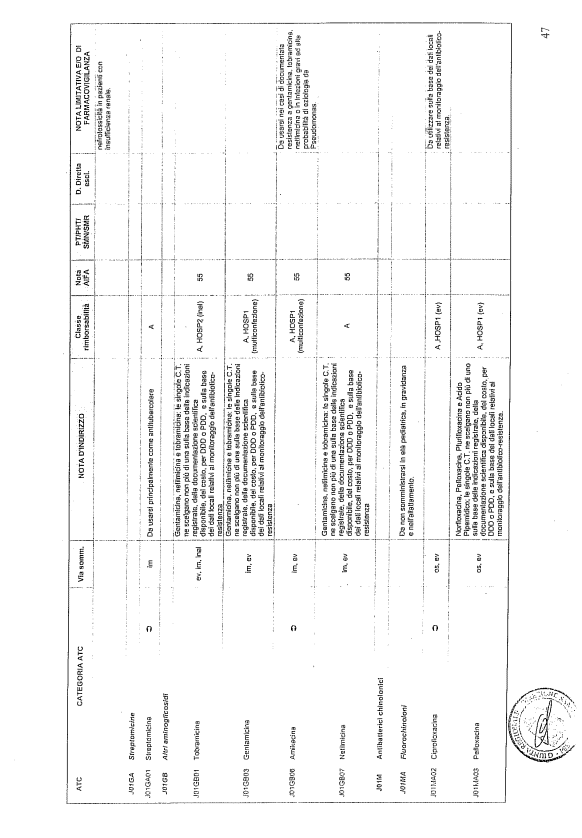
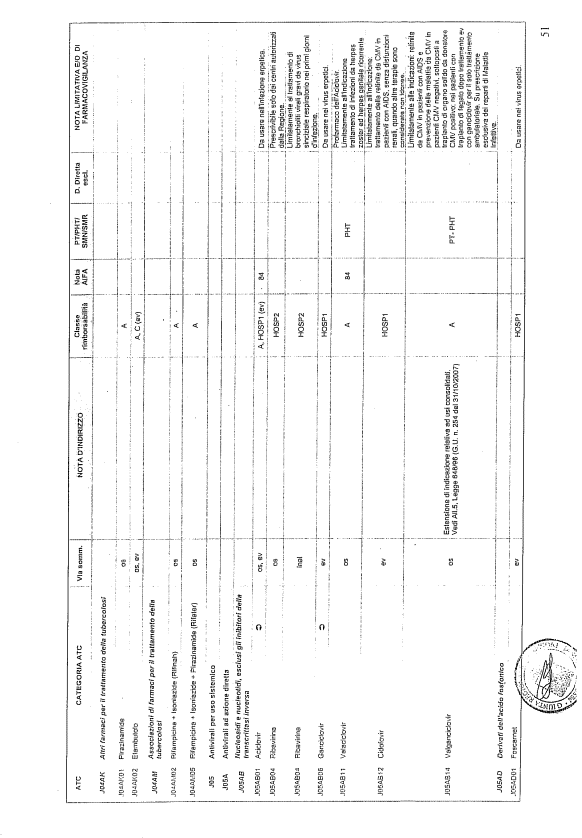
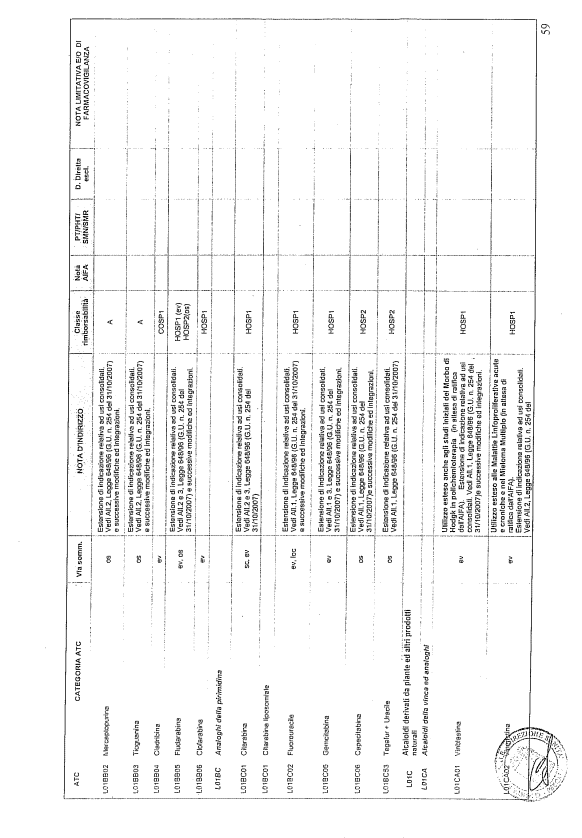
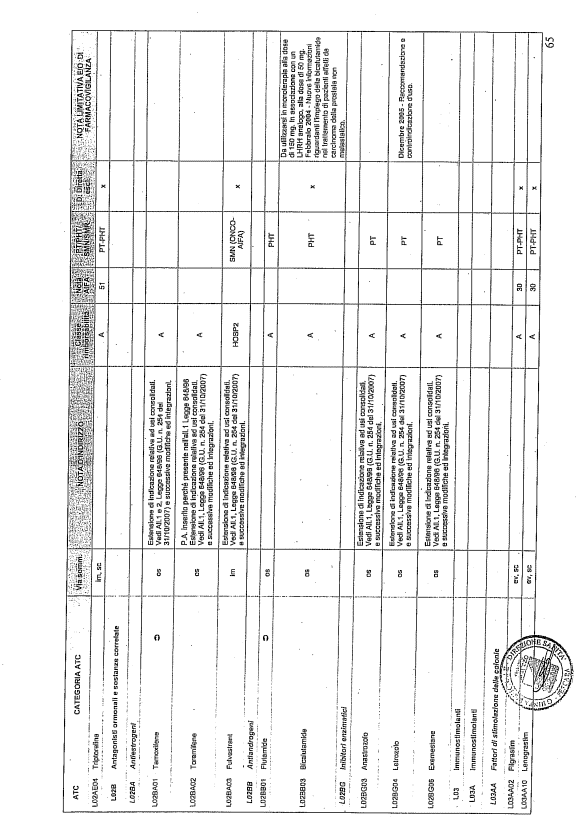
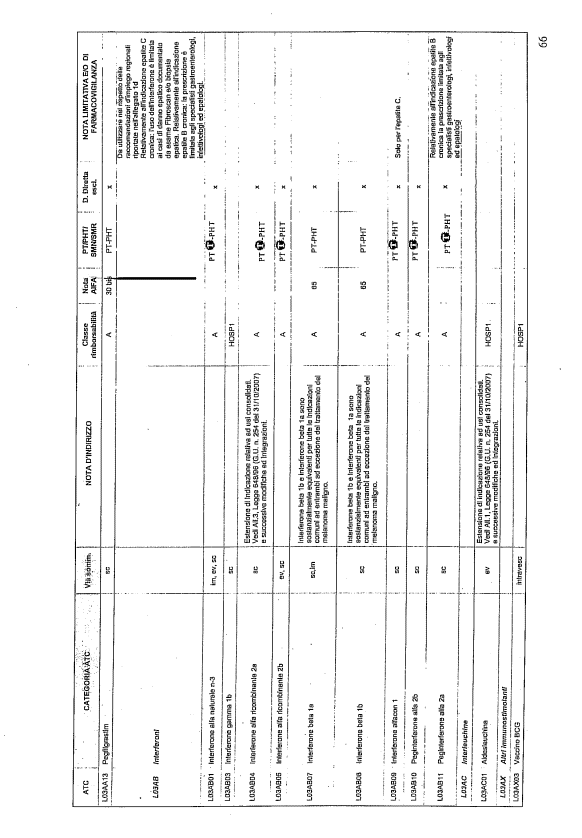
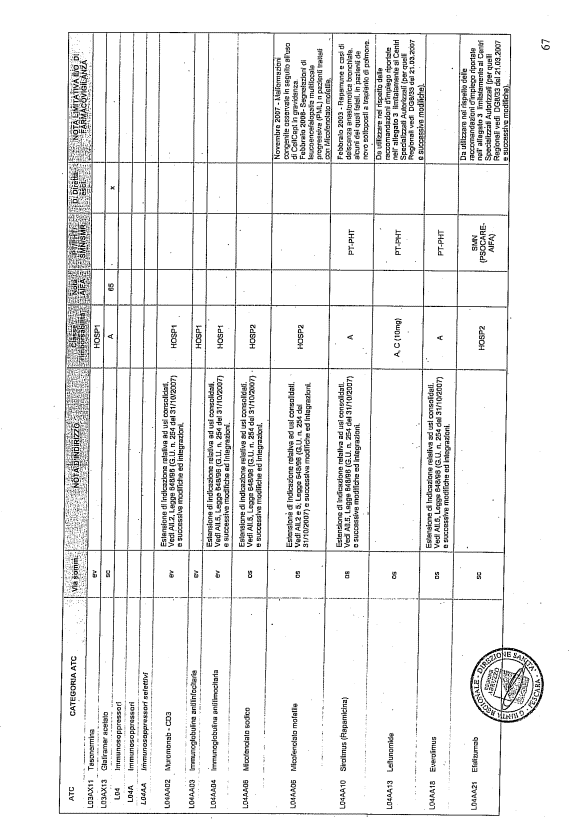
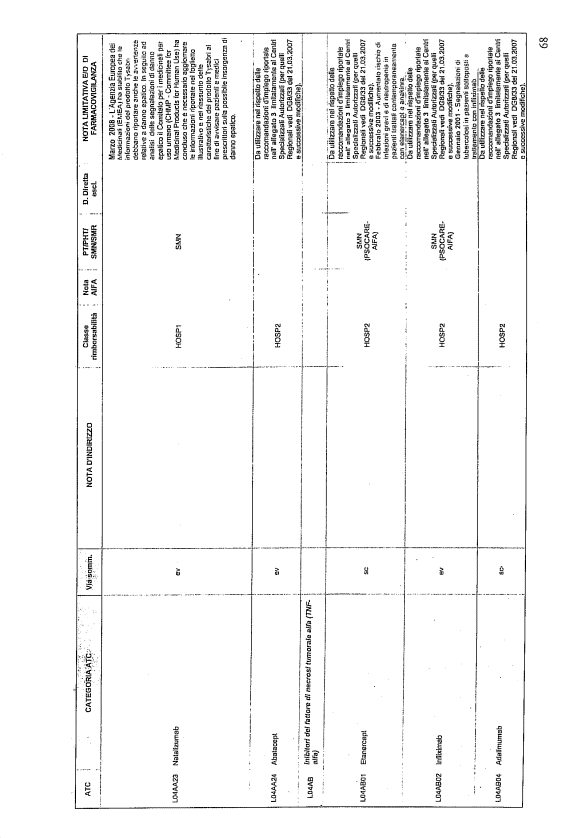
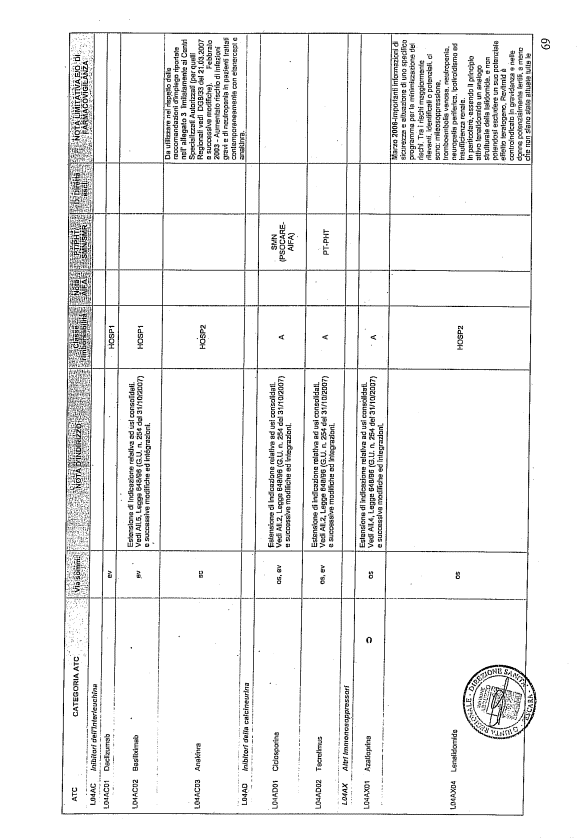
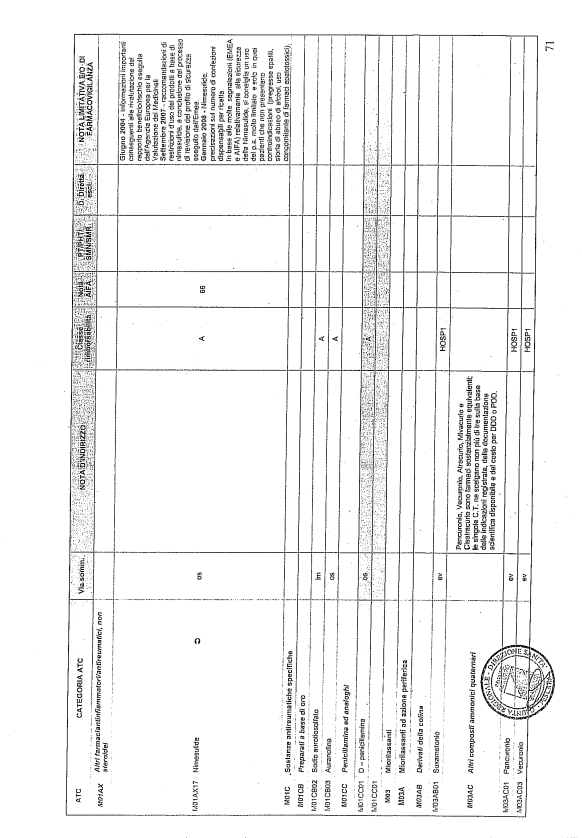
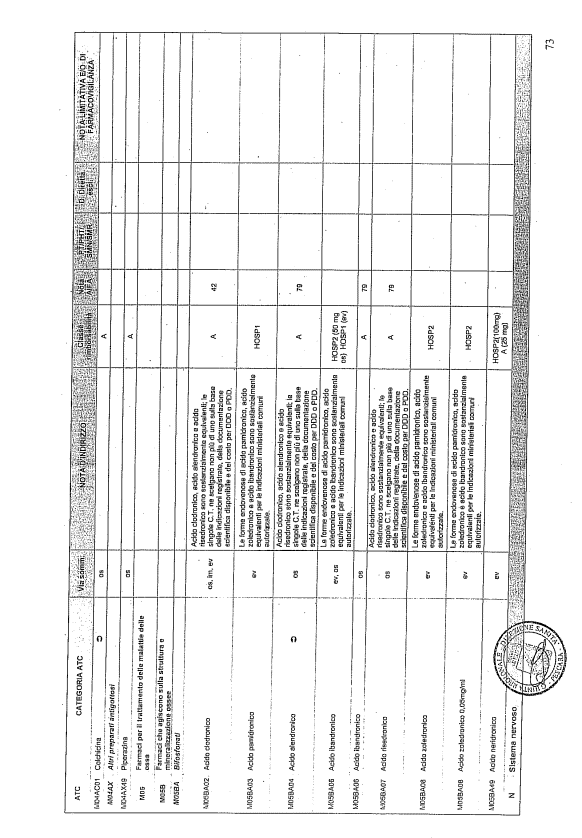
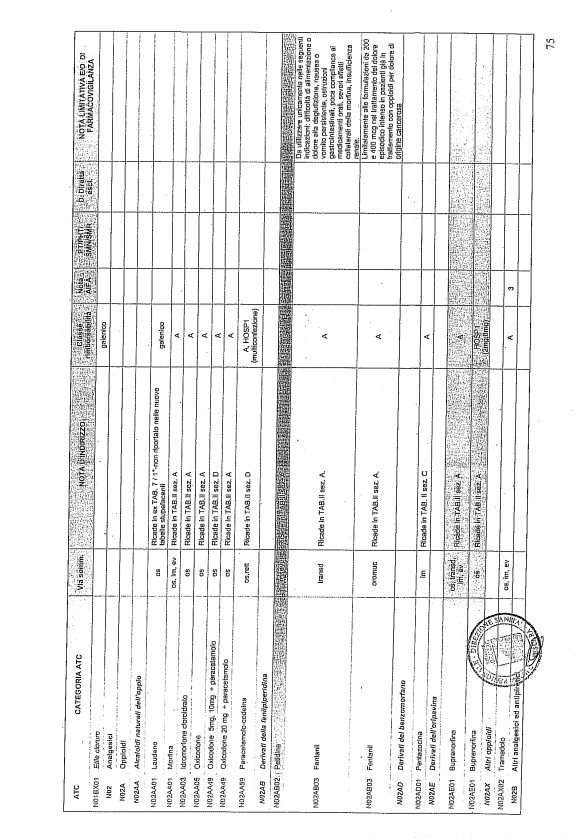
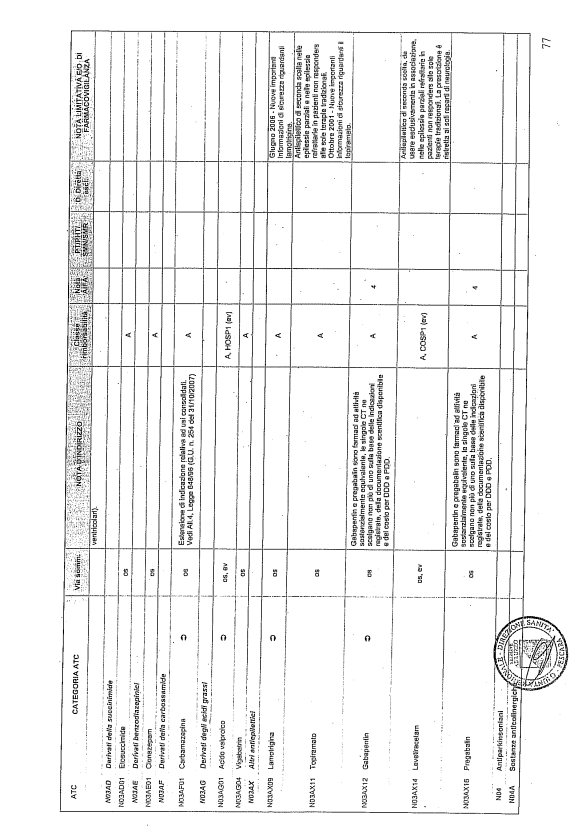
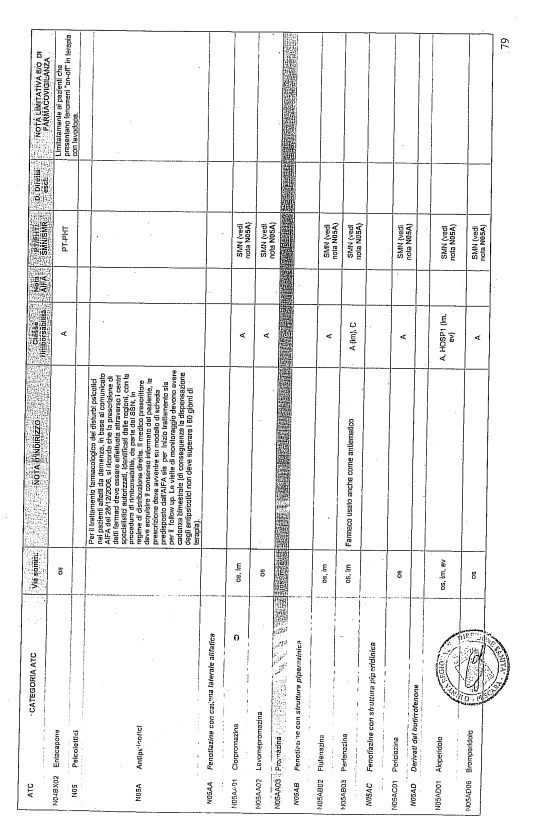
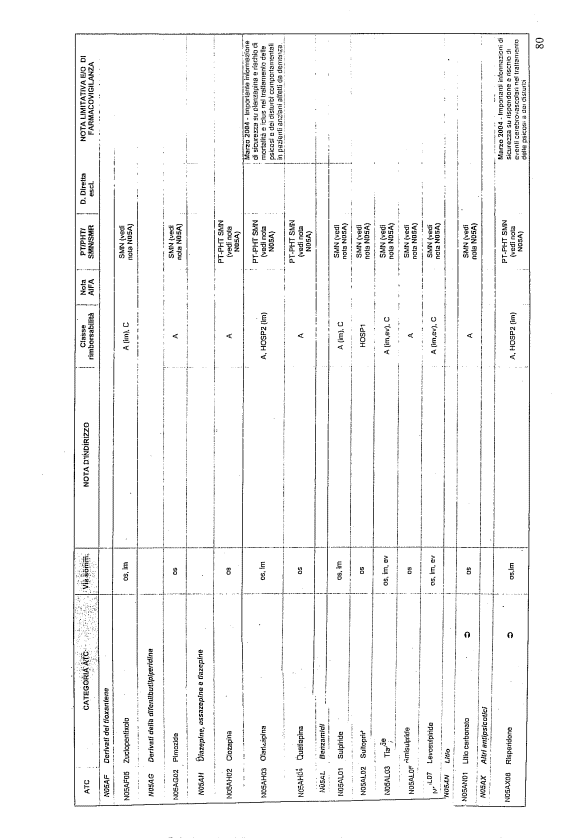
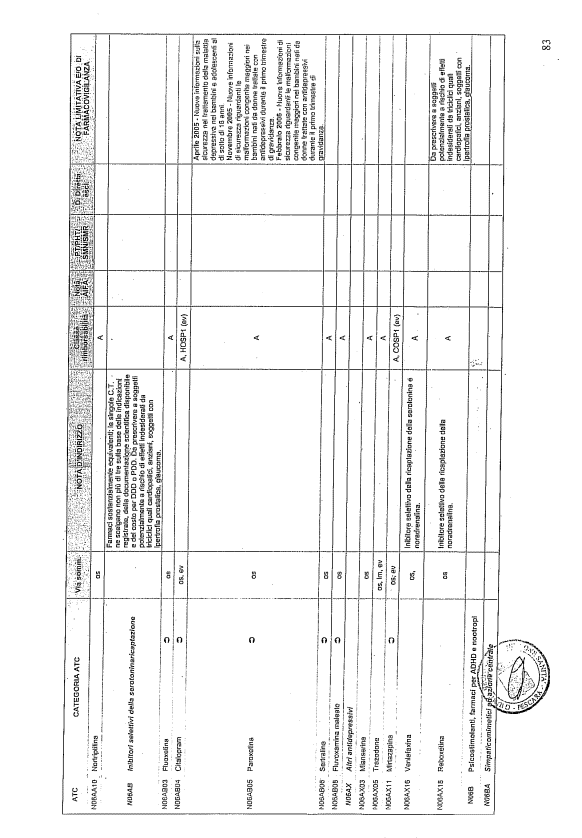
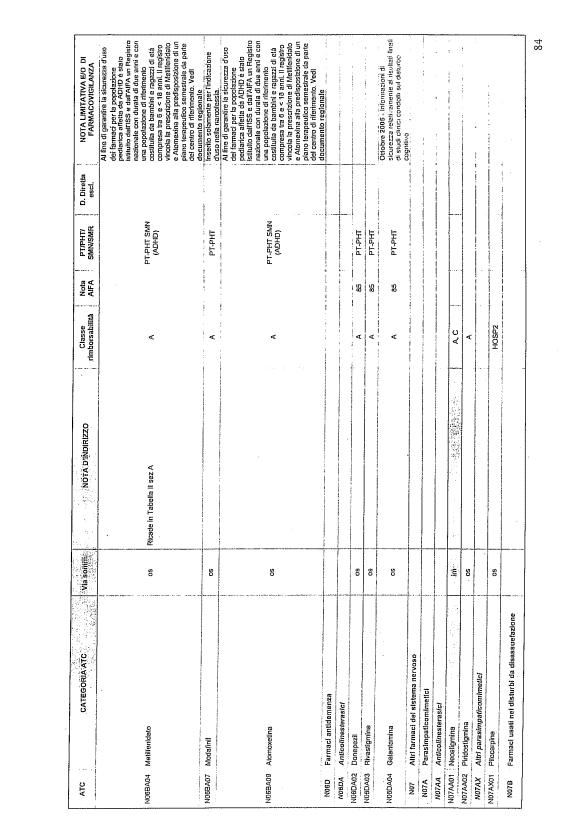
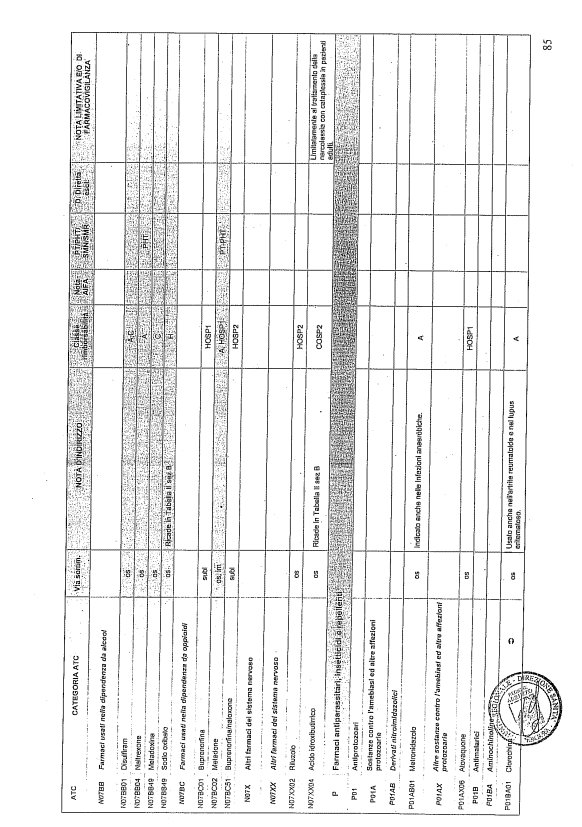
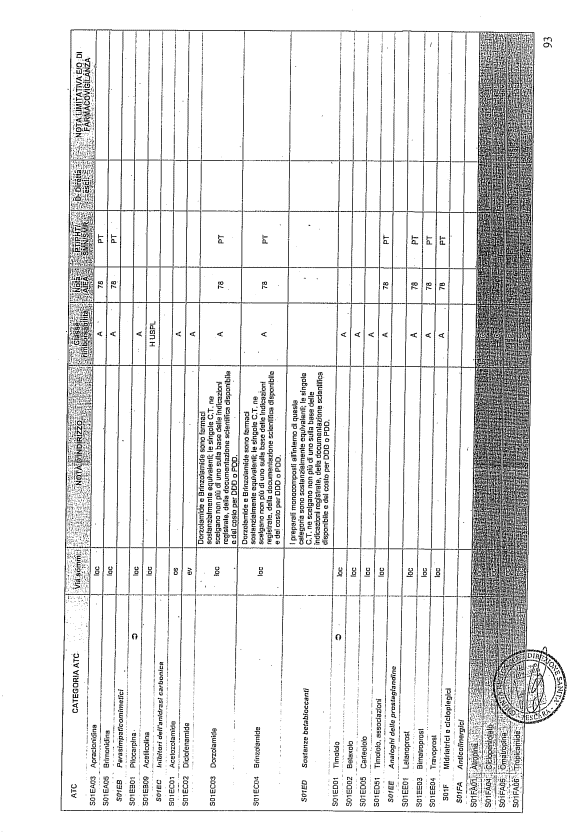
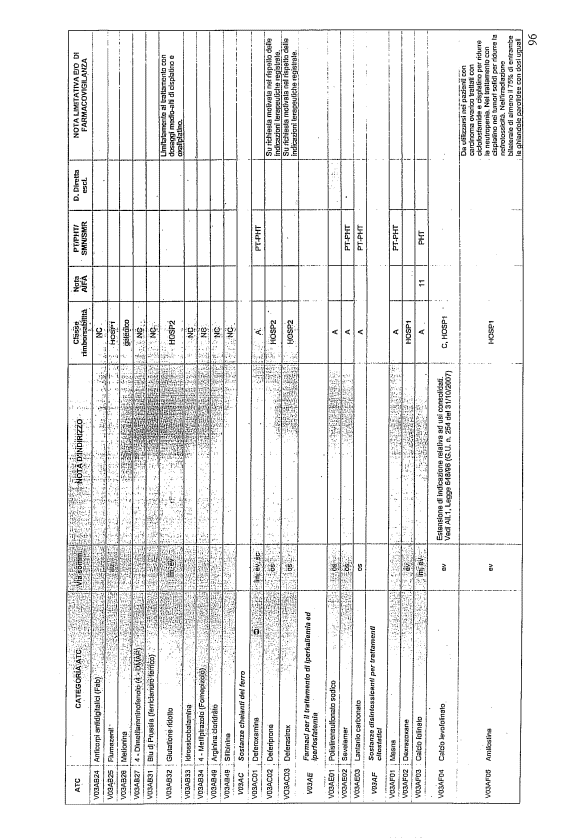
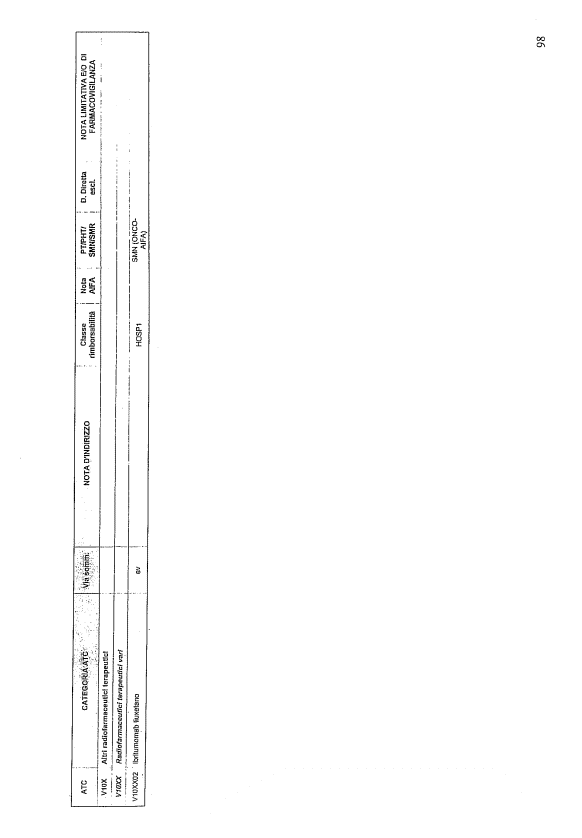
- PTR propriamente detto, contenente:
- un elenco di farmaci suddiviso secondo la classificazione ATC;
- note che indirizzino le Commissioni farmaceutiche aziendali ed i medici prescrittori nella scelta o nella prescrizione del principio attivo indicato;
- la necessità di eventuale Piano terapeutico secondo le disposizioni AIFA;
- la necessità di eventuale monitoraggio effettuato mediante schede nazionali e/o regionali;
- l’eventuale inserimento nel PHT (Prontuario della continuità ospedale-territorio;
- l’eventuale distribuzione diretta esclusiva;
- le note limitative e/o di farmacovigilanza;
- Appendici:
1. elenco dei gruppi terapeutici per i quali le singole Commissioni Terapeutiche sono invitate a scegliere un numero più ristretto di principi attivi;
2. elenco dei principi attivi genericati e relativi prezzi di riferimento regionali;
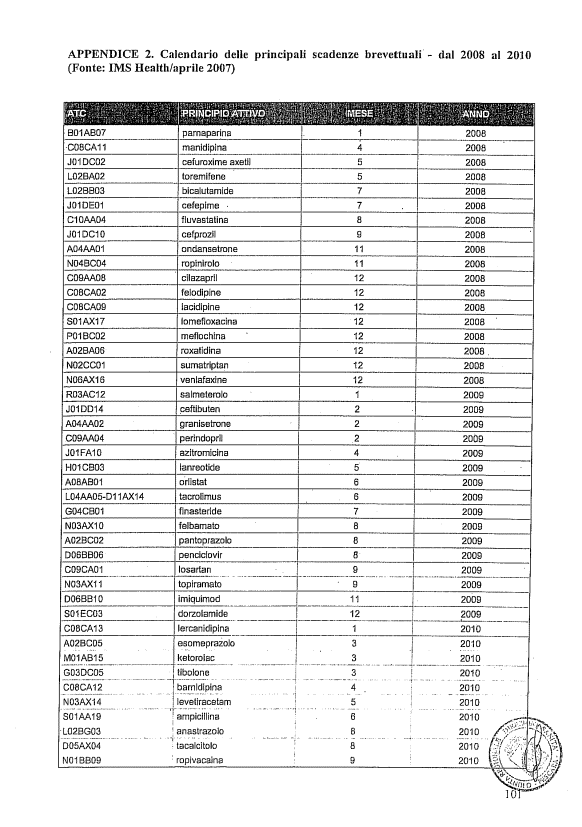
3. calendario delle principali scadenze brevettuali dal 2008 al 2010;
- Allegati:
1. Note preliminari per la definizione di indicazioni regionali all’impiego di farmaci antinfettivi:
a. Terapia con farmaci antibiotici di nuova generazione;
b. Farmaci antiretrovirali per HIV;
c. Farmaci nucleosidici per trattamento epatite cronica;
d. Interferoni e farmaci correlati per trattamento infezione cronica da HCV e HBV;
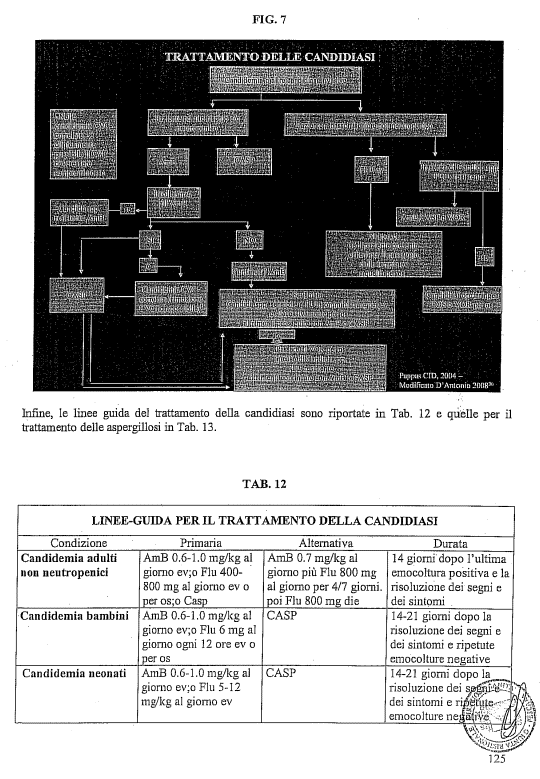
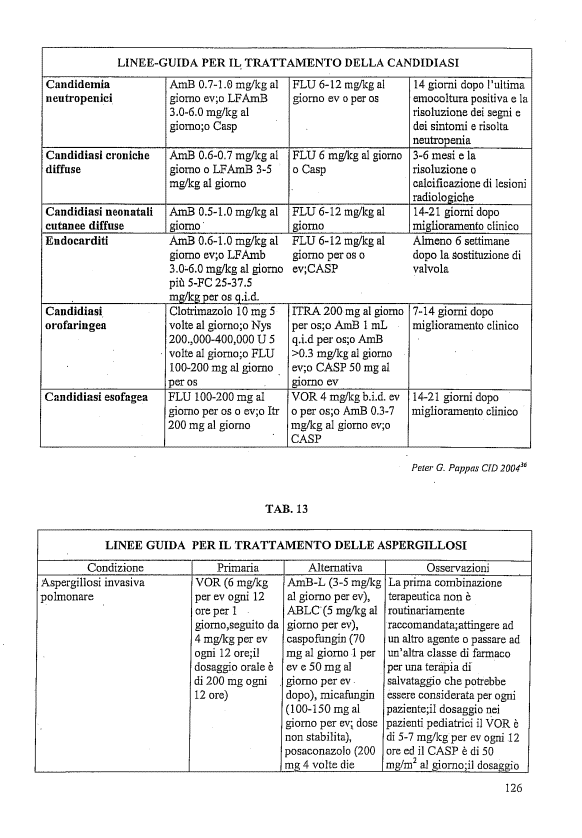
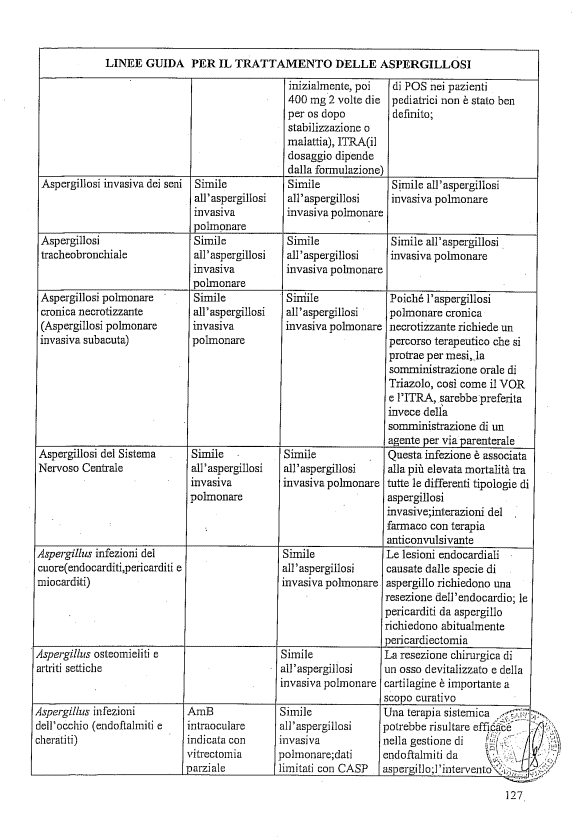
2. Percorso diagnostico terapeutico delle infezioni fungine;
3. DMARD’s, altri DMARD’s e BRM - Indicazioni e raccomandazioni di impiego;
- Modulistica
- Scheda di monitoraggio regionale per glitazoni;
- Piano terapeutico regionale per insulina glargine e insulina determir;
- Modulo di richiesta motivata regionale per farmaci antinfettivi;
- Moduli per richieste di inserimento nel PTR di nuovo farmaco o di nuova indicazione terapeutica;
Reputato di recepire integralmente il Prontuario siccome integrato e modificato, comprensivo delle Appendici ed Allegati di cui al punto precedente (all. 1), in quanto rispondente all’Obiettivo L1 del Piano di risanamento del Sistema Sanitario Regionale 2007/2009 - punto 2.1.3.1.5.;
Richiamato l’art. 1 comma 2 della L. R. 30 dicembre 2003, n. 27 “Norme in materia di monitoraggio delle prescrizioni mediche, farmaceutiche, specialistiche ed ospedaliere nella Regione Abruzzo” ove viene espressamente stabilito che “...l’erogazione a carico del SSN è esclusa per le prestazioni: ... b) che non soddisfano i principi di efficacia e di appropriatezza, o la cui efficacia non sia dimostrabile in base a criteri scientifici, o che siano utilizzate per soggetti le cui condizioni cliniche non corrispondono alle indicazioni raccomandate...”;
Atteso che nei diversi gruppi terapeutici è stato proposto un numero di principi attivi rispetto ai quali è raccomandata alle singole Commissioni Terapeutiche aziendali una puntuale selezione (cfr. appendice 1 del PTR), sia tenendo conto delle diverse realtà assistenziali locali, sia al fine di garantire la necessaria continuità assistenziale durante il ricovero, alla dimissione e sul territorio;
Richiamate altresì le Linee Guida per la stesura dei Piani Strategici Aziendali - approvate con D.G.R. n. 1115 del 09.10.2006 - ove, tra gli obiettivi strategici viene posta prioritariamente l’individuazione, da parte delle AA.SS.LL. di un articolato piano d’intervento per la ottimizzazione dell’erogazione dell’assistenza farmaceutica, sia a livello ospedaliero che territoriale, disponendo tra l’altro che l’inserimento dei farmaci nei prontuari terapeutici ospedalieri avvenga esclusivamente secondo criteri di efficacia e di giusta determinazione del costo/terapia;
Atteso che il Prontuario siccome aggiornato alla data del 14.05.2008, risulta composto - oltre che dall’elenco dei farmaci propriamente detto - da specifiche Schede di monitoraggio e Piani Terapeutici regionali per taluni farmaci antidiabetici, al fine di monitorare la popolazione trattata e verificare l’appropriatezza prescrittiva degli stessi, nonché da Moduli di richiesta motivata regionale per taluni farmaci antinfettivi, allo scopo di controllare da un punto di vista epidemiologico sia l’efficacia che l’evoluzione delle resistenza di alcune molecole appartenenti alla classe degli antimicrobici;
Reputato il PTR - oltre che un notevole veicolo e promotore di formazione culturale - un importante strumento di programmazione e di governo dell’assistenza farmaceutica, resa sia in ambito ospedaliero che sia a livello di continuità assistenziale sul territorio;
Ritenuto quindi opportuno nonché necessario - disporre per le AA.SS.LL.:
- l’obbligo dell’introduzione della modulistica sopracitata al fine della prescrizione dei farmaci e della relativa erogazione a carico del SSN;
- l’obbligo della selezione dei principi attivi da utilizzare tra quelli riportati nell’elenco di cui all’appendice 1 al PTR e la relativa comunicazione della selezione effettuata al Servizio Assistenza Distrettuale - Assistenza Farmaceutica della Direzione Sanità;
Richiamata la D.G.R. n. 675 del 18.07.2005 - successivamente integrata e modificata dalla D.G.R. n. 114 del 12.02.2007 e dalla D.G.R. n. 1349 del 27.12.2007 - recante la Istituzione della Rete Regionale di Centri di Informazione Indipendente sui Farmaci, la quale ha, tra l’altro, previsto l’attivarsi di specifico sito web (www.farmaci.abruzzo.it) dedicato all’informazione scientifica indipendente sui farmaci della Regione Abruzzo, nell’ambito del quale fosse resa pubblica l’attività della Commissione Regionale del Farmaco;
Ritenuto quindi opportuno - al fine di consentire la tempestiva consultazione del PTR nei suoi costanti aggiornamenti agli operatori sanitari ed a tutti i soggetti ad ogni titolo interessati - rendere disponibile la consultazione on line sul sito web www.farmaci.abruzzo.it di tutta la documentazione prodotta dalla CRF;
Dato atto che il Direttore Regionale della Direzione Sanità ed il Dirigente del Servizio Assistenza Distrettuale - Assistenza Farmaceutica hanno espresso parere favorevole in ordine rispettivamente alla legittimità ed alla regolarità tecnica ed amministrativa del presente provvedimento;
A voti unanimi espressi nelle forme di legge,
deLiBeRA
per le motivazioni espresse in narrativa
1. di recepire i criteri di elaborazione del Prontuario Terapeutico Regionale siccome definiti dalla Commissione Regionale del Farmaco – e già recepiti, ai sensi e per gli effetti della L.R. 77/1999, da provvedimento dirigenziale DG8/111 del 24.10.2007 - espressamente resi nell’allegato A al presente provvedimento, di cui costituisce parte integrante e sostanziale,
2. di recepire il Prontuario Terapeutico della Regione Abruzzo reso nell’allegato 1 al presente atto, di cui costituisce parte integrante e sostanziale, siccome implementato ed integrato dalla Commissione Regionale del Farmaco nel corso della seduta tenutasi in data 14.05.2008 e recepito con DG8/71 del 29.05.2008;
3. di disporre che i Direttori Generali delle AA.SS.LL. provvedano affinché - entro 60 giorni dalla data di adozione del presente atto - in ogni ASL della Regione sia istituita ed attivata la Commissione farmaceutica aziendale al fine di rendere possibile tutte le attività necessarie ad una corretta politica nel campo dell’assistenza farmaceutica - sia essa ospedaliera che territoriale - ed una corretta e proficua interazione con la Commissione Regionale del farmaco;
4. di disporre che i Direttori Generali delle AA.SS.LL. provvedano affinché - al fine della prescrizione dei farmaci interessati e della relativa erogazione a carico del SSN - sia resa vincolante all’interno delle AA.SS.LL. l’introduzione della modulistica riportata nel Prontuario Terapeutico dì cui al precedente punto 2;
3. di disporre che i Direttori Generali delle AA.SS.LL. provvedano affinché entro 60 giorni dalla data di adozione del presente atto - sia comunicata alla Commissione Regionale del Farmaco, per il tramite del Servizio Assistenza Farmaceutica della Direzione Sanità - la selezione dei principi attivi effettuata tra quelli riportati nell’elenco di cui all’appendice 1 al PTR;
6. di demandare al Servizio Assistenza Distrettuale - Assistenza Farmaceutica della Direzione Sanità:
a) di effettuare presso le Aziende Sanitarie Locali della Regione Abruzzo una ricognizione in merito ad eventuali elementi di difformità dei Prontuari vigenti - laddove predisposti - rispetto al Prontuario Terapeutico Ospedaliero della Regione Abruzzo siccome approvato e reso nell’allegato 1 al presente atto;
b) di stabilire le modalità e la cadenza con cui i Servizi Farmaceutici Territoriali delle AA.SS.LL. e le Farmacie dei PP.OO. provvedono a trasmettere al Servizio Assistenza Distrettuale - Assistenza Farmaceutica della Direzione Sanità i dati relativi al monitoraggio effettuato con la modulistica di cui al punto 2;
4. di prendere atto che il Servizio Assistenza Distrettuale - Assistenza Farmaceutica della Direzione Sanità provvederà:
a) alla gestione ed alla revisione del PTR - avvalendosi del supporto della Commissione Regionale del Farmaco e del Centro di Informazione Indipendente sui Farmaci - recependone gli aggiornamenti con apposito provvedimento Dirigenziale;
b) ad integrare, su proposta della Commissione Regionale del Farmaco, il PTR di cui al precedente punto 2 - relativamente ad alcuni farmaci per cui siano richieste particolari precauzioni d’uso legate al profilo di sicurezza ed alla maneggevolezza del farmaco stesso, ovvero siano destinati ad una particolare fascia di pazienti, o ancora abbiano un costo molto elevato - con specifiche note limitative o schede di richiesta motivata o schede di monitoraggio, al fine di verificare puntualmente che il farmaco sia prescritto ed utilizzato nelle condizioni autorizzate;
c) a rendere consultabile on line gli aggiornamenti del PTR approvato con il presente atto, sul sito della Regione Abruzzo appositamente dedicato all’informazione indipendente sui Farmaci www.farmaci.abruzzo.it;
5. di
disporre la notifica del presente atto ai Direttori Generali della AA.SS.LL.,
affinché ne diano la massima diffusione agli operatori sanitari interessati,
nonché la pubblicazione dello stesso sul Bollettino
Ufficiale della Regione, sul Portale della Sanità della Regione Abruzzo e
sul sito della Regione Abruzzo appositamente dedicato all’Informazione
indipendente sui Farmaci www.farmaci.abruzzo.it.
Seguono allegati